能级原理
-
光电效应与能级跃迁原理
原始称呼是光量子(light quantum),电磁辐射的量子,传递电磁相互作用的规范粒子,记为γ。其静止量为零,不带荷电,其能量为普朗克常量和电磁辐射频率的乘积,ε=hv,在真空中以光速c运行,其自旋为1,是玻色子。早在1900年,M.普朗克解释黑体辐射能量分布时作出量子假设,物质振子与辐射之间的能量交换是不连续的,一份一份的,每一份的能量为hv;1905年A.爱因斯坦进一步提出光波本身就不是连续的而具有粒子性,爱因斯坦称之为光量子;1923年A.H.康普顿成功地用光量子概念解释了X光被物质散射时波长变化的康普顿效应,从而光量子概念被广泛接受和应用,1926年正式命名为光子。量子电动力学确立后,确认光子是传递电磁相互作用的媒介粒子。带电粒子通过发射或吸收光子而相互作用,正反带电粒子对可湮没转化为光子,它们也可以在电磁场中产生。
光子是光线中携带能量的粒子。一个光子能量的多少与波长相关, 波长越短, 能量越高。当一个光子被分子吸收时,就有一个电子获得足够的能量从而从内轨道跃迁到外轨道,具有电子跃迁的分子就从基态变成了激发态。简易物理 回复于:2021-07-12 14:08:08 -
玻尔原子理论的基本假设
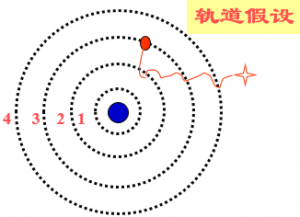
1、轨道假设
原子中的电子在库仑力的作用下,绕原子核做圆周运动,服从经典力学的规律。但是,电子轨道半径不是任意的,只有当半径大小符合一定条件时,这样的轨道才是可能的。即电子的轨道是量子化的。 电子在这些轨道上绕核的转动是稳定的,不产生电磁辐射。
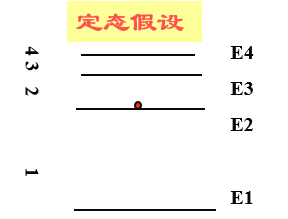
2、能级假设
当电子在不同轨道上运动时,原子处于不同状态,具有不同能量,所以原子能量也是量子化的。
这些量子化的能量值叫能级;原子中这些具有确定能量的稳定状态叫定态。
能量最低的状态叫基态,其他状态叫激发态。
下图是氢原子基态(第一能级)与激发态之间的等量关系:
$E_n = \frac{1}{n^2}E_1$
其中En表示第n能级的能量,E1表示基态(第一能级),$E_1=-13.6eV$
3、跃迁假设
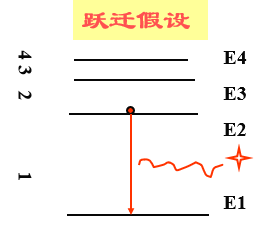
当电子从能量较高的定态轨道(设能量为Em)跃迁到能量较低的定态轨道(设能量为En,m>n)时,它辐射出一定频率的光子,光子的能量由这两种定态的能量差决定,即
$hν = E_m - E_n$
同样的,当电子吸收光子时会从较低的能量态跃迁到较高的能量态,吸收的光子的能量同样由两种定态的能量差决定。

电离:完全脱离原子核束缚,电离条件:$hν≥E_n$。电离后电子剩余动能为:
$E_k = hν + E_n = hν - |E_n|$
简易物理 回复于:2021-07-12 14:09:07