能级数
-
能级级数
在每个能层中,能级符号的顺序是 (n代表能层)。任意能层总是从 能级开始,而且能级数等于 ,第一能层只有 个能级,能级符号 ,第二能层有 个能级,能级符号 ,第三能层有 个能级,能级符号 ,等等。以 排序的各能级可容纳的最多电子数依次是 (与能级对应)
ns np nd nf ;s;能层序数;1;1s;2;2s2p;3;3s3p3d;spdf;2 6 10 14
--转自百度知道
简易物理 回复于:2021-07-12 14:37:30 -
玻尔原子理论的基本假设
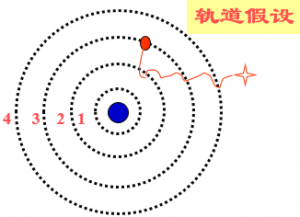
1、轨道假设
原子中的电子在库仑力的作用下,绕原子核做圆周运动,服从经典力学的规律。但是,电子轨道半径不是任意的,只有当半径大小符合一定条件时,这样的轨道才是可能的。即电子的轨道是量子化的。 电子在这些轨道上绕核的转动是稳定的,不产生电磁辐射。
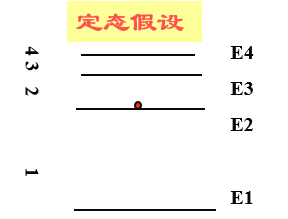
2、能级假设
当电子在不同轨道上运动时,原子处于不同状态,具有不同能量,所以原子能量也是量子化的。
这些量子化的能量值叫能级;原子中这些具有确定能量的稳定状态叫定态。
能量最低的状态叫基态,其他状态叫激发态。
下图是氢原子基态(第一能级)与激发态之间的等量关系:
$E_n = \frac{1}{n^2}E_1$
其中En表示第n能级的能量,E1表示基态(第一能级),$E_1=-13.6eV$
3、跃迁假设
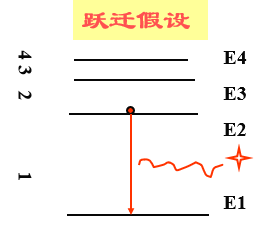
当电子从能量较高的定态轨道(设能量为Em)跃迁到能量较低的定态轨道(设能量为En,m>n)时,它辐射出一定频率的光子,光子的能量由这两种定态的能量差决定,即
$hν = E_m - E_n$
同样的,当电子吸收光子时会从较低的能量态跃迁到较高的能量态,吸收的光子的能量同样由两种定态的能量差决定。

电离:完全脱离原子核束缚,电离条件:$hν≥E_n$。电离后电子剩余动能为:
$E_k = hν + E_n = hν - |E_n|$
简易物理 回复于:2021-07-12 14:37:41 -
相关链接:
简易物理 回复于:2022-02-25 04:22:06 -
简易物理 回复于:2022-02-25 04:24:10