克拉伯龙方程
-
克拉伯龙方程描述的是单元系在一阶相变相平衡时候物理量的变化方程。即定量分析单元系在摩尔数相同时物质体积(V)、温度(T)、压强(p)的关系
$\frac{dp}{dT}=\frac{L}{TΔV}$
其中是相变潜热,是比体积或摩尔体积的变化。
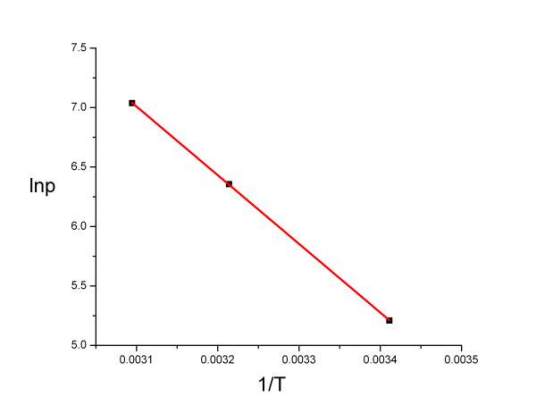 简易物理 回复于:2022-09-04 19:08:41
简易物理 回复于:2022-09-04 19:08:41 -
由克拉伯龙于将玻意耳定律和盖-吕萨克定律合并起来。特此澄清一点,部分国内教材将理想气体状态方程和克拉伯龙方程画等号,这是不正确的。
尽管理想气体状态方程是由克拉伯龙提出的,但是克拉伯龙方程所描述的是相平衡的物理量。国际惯例,将理想气体状态方程称为State Equation of Ideal Gas 或者 Ideal Gas law。
而克拉伯龙方程 Clapeyron Equation的同义词是 Clausius-Clapeyron Relation 或者 Clapeyron Equation.大量百度知道和之前的百度百科混淆了这一点。
简易物理 回复于:2022-09-04 19:11:31 -
克拉伯龙方程描述的是单物质在一阶相变相平衡时候物理量的变化方程。即定量分析单物质在摩尔数相同时物质体积(V)、温度(T)、压强(P)的关系。方程
$pV=nRT$。
4个变量分别为:p是指理想气体的压强,
V为理想气体的体积,
n表示气体物质的量,
而T则表示理想气体的热力学温度;还有一个常量:R为理想气体常数。
可以看出,此方程的变量很多。此方程以其变量多、适用范围广而著称,对常温常压下的空气也近似地适用。
值得注意的是,把理想气体方程和克拉伯龙方程等效是不正确的。一般克拉伯龙方程是指描述相平衡的方程$dp/dT=L/(TΔv)$。尽管理想气体定律是由克拉伯龙提出,但是国际上不把理想气体状态方程叫克拉伯龙方程。
简易物理 回复于:2022-09-04 19:14:10